
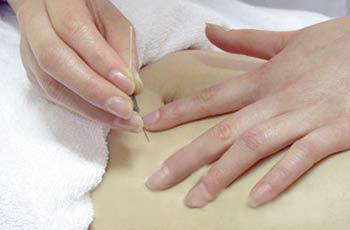
Cấy chỉ là một phương pháp chữa bệnh không dùng thuốc đặc biệt, độc đáo của châm cứu Việt Nam, bao gồm chôn chỉ, vùi chỉ, xuyên chỉ, thắt buộc chỉ. Là một phương pháp châm cứu mới, hiện đại áp dụng tiến bộ của khoa học kỹ thuật trên cơ sở kế thừa những lý luận và kinh nghiệm của châm cứu. Phương pháp này đó được áp dụng tại Việt Nam từ những năm 1960 của thế kỷ trước. Nhiều bệnh mạn tính đó được điều trị khỏi bằng phương pháp cấy chỉ.Không chỉ có giá trị ở Việt Nam mà còn nổi bật trên trường quốc tế, đặc biệt các nước châu âu, xứng đáng mang tên “cấy chỉ Việt”!

Thủy trị liệu là phương pháp sử dụng nước điều trị thông qua việc tác động lên bề mặt ngoài cơ thể.





Công Đoàn Bệnh viện Chúc mừng ngày Quốc tế Phụ nữ 08/03
Xem chi tiết









Thư mời chào giá về việc cung cấp máy lạnh công suất 1 HP của Bệnh viện Y học cố truyền - Phục hồi chức năng tỉnh Bình Thuận
Xem chi tiết

Thông báo về việc tuyển dụng lao động
Xem chi tiết

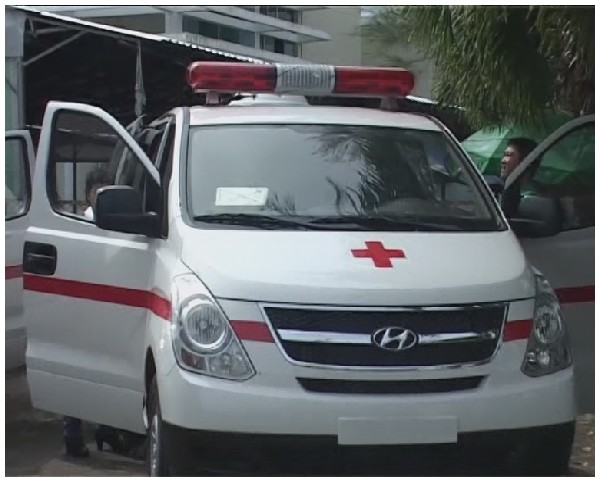
Cung ứng đầy đủ,kịp thời và cập nhật những trang thiết bị hiện đại về y học cổ truyền
Xem chi tiết
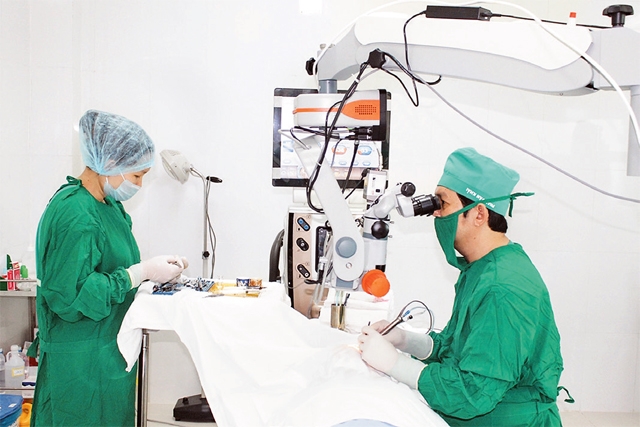
Ứng dụng kỹ thuật tiên tiến,hiện đại các phương thuốc cổ truyền
Xem chi tiết

Kết hợp y học cổ truyền và y học hiện đại để chữa bệnh
Xem chi tiết


